Qual é a diferença entre dureza temporária e permanente e isso importa para a preparação do café?
A dureza é uma medida da quantidade de certos minerais na água. A quantidade e a proporção de minerais na água de preparo podem ter um efeito dramático no sabor do café, bem como afetar a probabilidade de a sua máquina de café expresso aumentar de escala, por isso vale a pena tentar entender alguns conceitos-chave.
O termo 'dureza' vem originalmente do efeito dos minerais da água sobre o sabão. Os minerais em água não filtrada ligam-se ao sabão e formam uma 'espuma' insolúvel, dificultando a formação de espuma e tornando o sabão menos eficaz na lavagem. A certa altura, as pessoas notaram que se a água fosse fervida antes de usar, a água ficaria menos dura, facilitando a lavagem. A dureza que pode ser removida pela fervura é chamada de dureza temporária, a dureza que permanece, não importa o quanto você ferva a água, é chamada de dureza permanente.
Portanto, a definição é fácil de lembrar, mas para realmente entender o que está acontecendo, precisamos saber um pouco sobre de que são feitos os minerais da água. Cada mineral que se dissolve na água é composto de íons, que são partículas eletricamente carregadas. O mineral sólido tem quantidades iguais de cargas positivas e negativas misturadas, de modo que as cargas se cancelam. Por exemplo, o sal de cozinha, cloreto de sódio, é composto de partes iguais de sódio carregado positivamente (Na+) e íons cloreto carregados negativamente (Cl–). Quando o mineral se dissolve em água, os íons se separam ('dissociar') e espalhe na água.
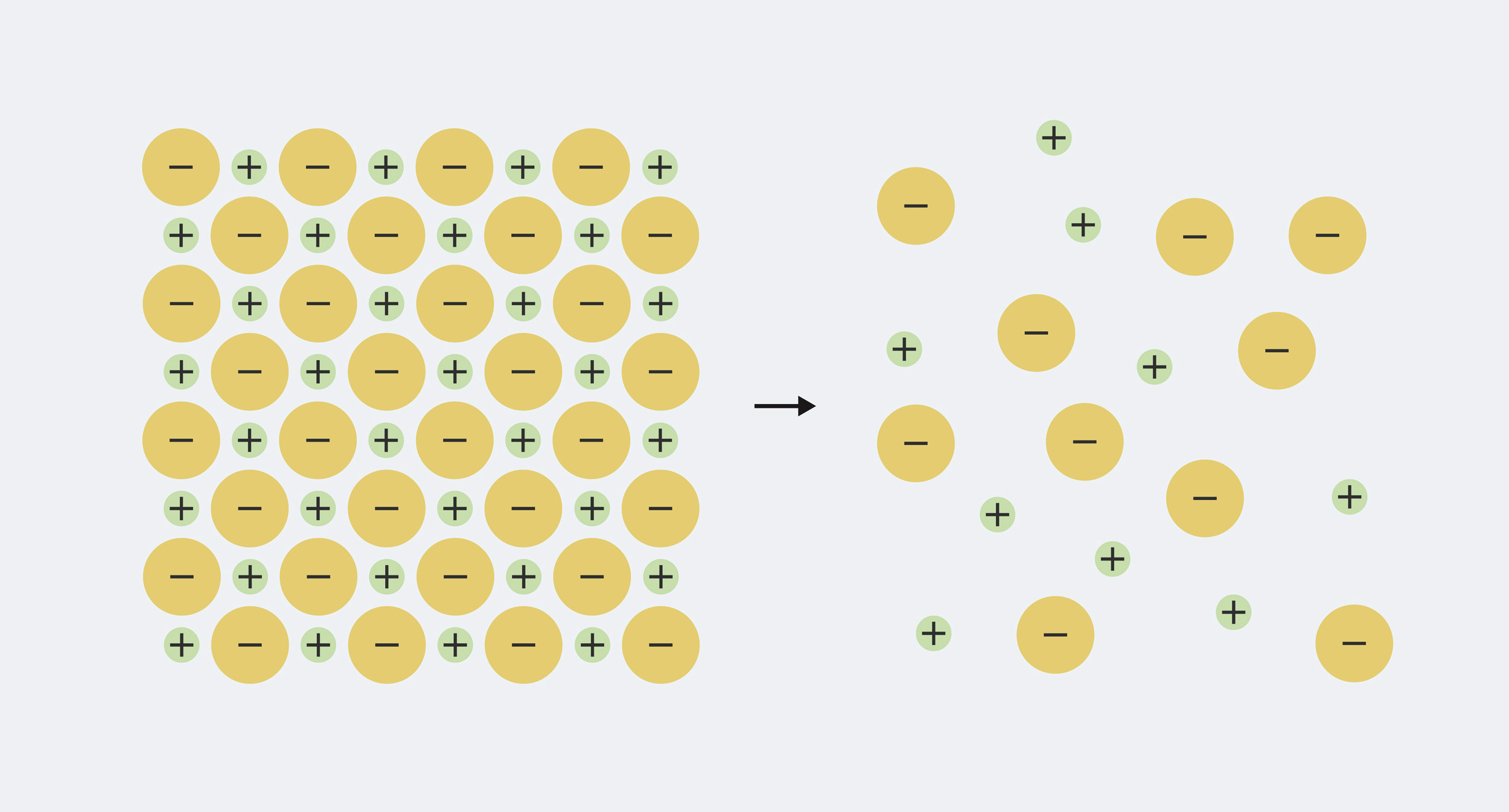 O sódio e o cloreto no sal de cozinha sólido são compactados juntos. Quando é dissolvido em água, separa-se em íons de sódio (Na+) e íons cloreto (Cl–)
O sódio e o cloreto no sal de cozinha sólido são compactados juntos. Quando é dissolvido em água, separa-se em íons de sódio (Na+) e íons cloreto (Cl–)
A dureza é causada por qualquer mineral onde o íon carregado positivamente tenha mais de uma carga. A carga mais forte destes iões é o que faz com que interajam com o sabão – e é a mesma carga que significa que estes minerais podem ajudar a extrair sabores do café.
Cálcio (Ca2+) e Magnésio (Mg2+) constituem quase toda a dureza da água potável. Como o cálcio e o magnésio possuem duas cargas positivas, eles se comportam de maneira muito semelhante, por isso podem ser considerados intercambiáveis quando falamos em dureza. Alguns outros íons, como o ferro (Fe3+) ou alumínio (Al3+), pode contribuir tecnicamente (OMS 2011), mas normalmente os ignoramos, pois a quantidade deles na água potável deve ser muito baixa.
Portanto, a dureza total, também chamada de “dureza geral” ou GH, é apenas uma medida da quantidade de cálcio e magnésio carregados positivamente que existe na água. Porque a carga elétrica nesses íons ajuda a extrair o sabor moléculas, a medição de GH é um indicador do poder de extração da água.
Agora lembre-se de que cada íon mineral com carga positiva também deve ser emparelhado com íons com carga negativa. O mais importante deles na água é o bicarbonato (HCO3–). Quando você ferve água com bicarbonato, ela reage com qualquer cálcio e magnésio da água para formar um sólido chamado calcário (carbonato de cálcio e carbonato de magnésio). Então é isso que causa a dureza temporária – ao ferver a água, você está formando calcário, que cai para o fundo. A dureza permanente é qualquer dureza que sobrar – qualquer cálcio ou magnésio que não tenha bicarbonato para reagir.
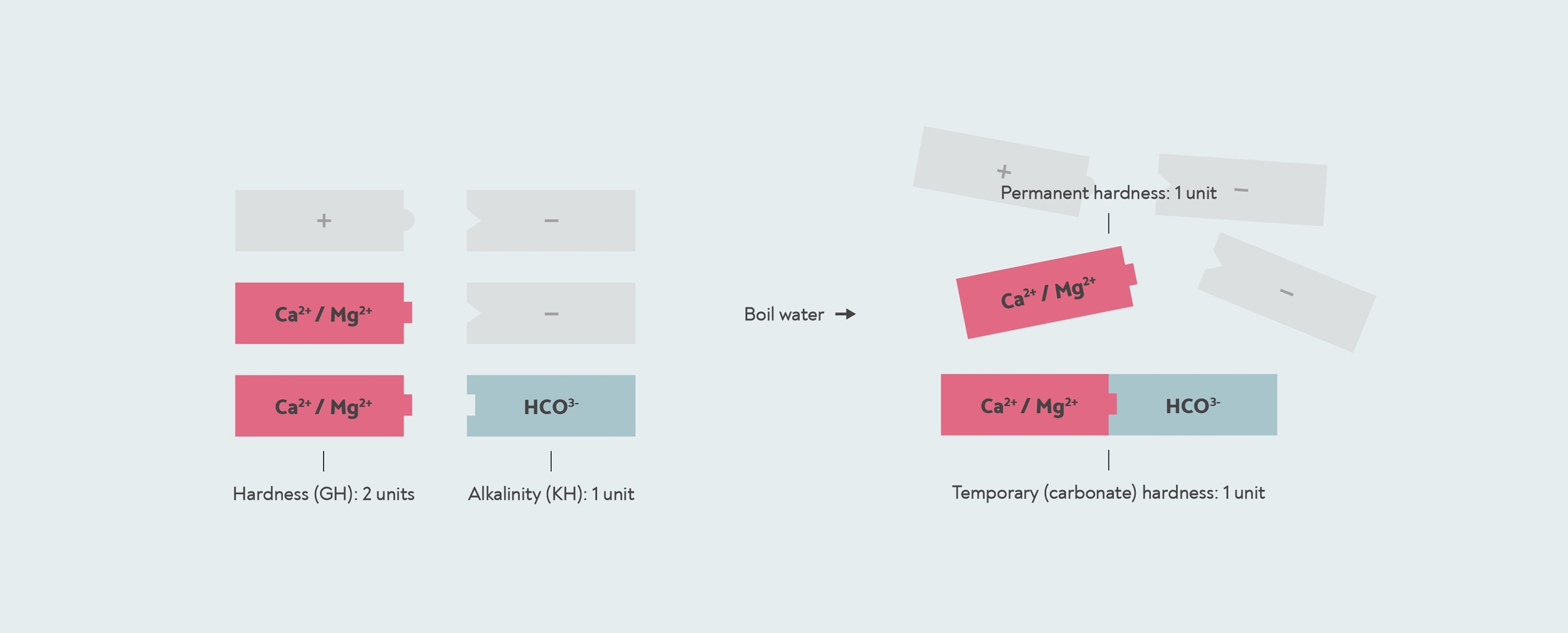 Dureza temporária e permanente. Essa água tem GH 2, pois contém duas unidades de cálcio/magnésio (vermelho). Tem uma dureza temporária de 1, porque uma unidade de carbonato se liga a uma unidade de cálcio/magnésio para formar calcário. O outro cálcio/magnésio é a dureza permanente que não se forma calcário e não é removido pela fervura. Os outros íons minerais positivos e negativos na água são mostrados em cinza.
Dureza temporária e permanente. Essa água tem GH 2, pois contém duas unidades de cálcio/magnésio (vermelho). Tem uma dureza temporária de 1, porque uma unidade de carbonato se liga a uma unidade de cálcio/magnésio para formar calcário. O outro cálcio/magnésio é a dureza permanente que não se forma calcário e não é removido pela fervura. Os outros íons minerais positivos e negativos na água são mostrados em cinza.
Quando medimos a dureza da nossa água, normalmente fazemos duas medições: GH e KH. GH é a dureza geral e mede a quantidade total de cálcio e magnésio na água. KH significa Karbonathärte, que significa dureza carbonatada em alemão. A dureza carbonatada é exatamente igual à dureza temporária: significa toda a dureza que está emparelhada com íons bicarbonato, que podem formar calcário.
No entanto, o que fica confuso é que um teste KH típico na verdade não mede a dureza do carbonato. Um teste de queda KH apenas mede a quantidade de bicarbonatos na água, também chamada de alcalinidade. Esta medida também é importante porque o alcalinidade buffers fora acidez no café e faz com que tenha um sabor menos ácido. Demais alcalinidade fará com que o sabor do café fique monótono.
Em nosso exemplo até agora, o alcalinidade é exatamente igual à dureza temporária, porque há cálcio e magnésio suficientes para reagir com todo o bicarbonato e formar calcário. Este é o caso da maior parte da água potável natural – a alcalinidade e a dureza do carbonato ou dureza temporária são exatamente as mesmas, então na maioria das vezes o teste KH também informa a dureza do carbonato.
Porém, em alguns casos, a quantidade de bicarbonato pode ser maior que a quantidade de cálcio ou magnésio. Isto pode acontecer quando a água foi amaciada ou quando a água salgada entrou na água potável. Neste caso, pode não haver cálcio e magnésio suficientes para reagir com todo o bicarbonato. Com esse tipo de água, se você ferver, toda a dureza é removida, então a dureza temporária é igual à dureza total, e não há nenhuma dureza permanente.
Neste caso, o teste KH lhe dará um resultado superior ao seu GH. Quando o resultado de um teste KH é superior ao GH, então a dureza do carbonato e a dureza geral são na verdade as mesmas. O número que o teste KH fornece é, na verdade, o alcalinidade, não a dureza do carbonato.
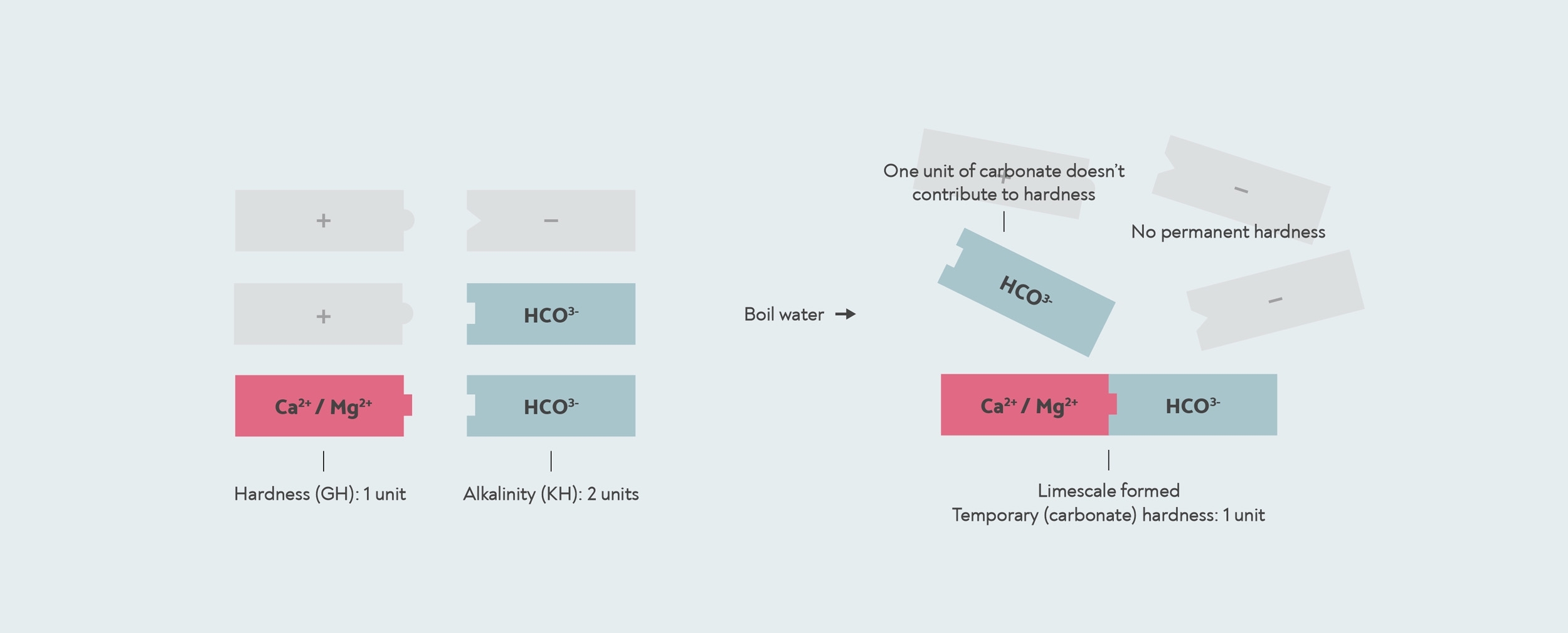 Quando o alcalinidade é maior que a dureza geral, então toda a dureza é temporária ou dureza carbonatada. Neste caso, o restante alcalinidade não contribui para a dureza. O kit de queda KH mede uma alcalinidade de 2, mas a dureza do carbonato é na verdade apenas 1, porque existe apenas 1 unidade de dureza para ele se formar calcário com.
Quando o alcalinidade é maior que a dureza geral, então toda a dureza é temporária ou dureza carbonatada. Neste caso, o restante alcalinidade não contribui para a dureza. O kit de queda KH mede uma alcalinidade de 2, mas a dureza do carbonato é na verdade apenas 1, porque existe apenas 1 unidade de dureza para ele se formar calcário com.
Este caso é bastante raro na água da torneira, porém, a maioria de nós pode ignorá-lo quando estamos testando nossa água. Na maior parte da água potável, KH = alcalinidade = dureza temporária. A dureza permanente é qualquer dureza que sobrou, então: Dureza Permanente = GH - KH.
Em resumo, estas são as três medidas que realmente importam na preparação do café: a dureza total ou dureza geral (GH), a dureza temporária, ou dureza carbonática, e a alcalinidade. A dureza total ajuda a água a extrair o sabor do café. A dureza temporária é o que determina quanto dessa dureza pode se formar calcário. finalmente, o alcalinidade determina quanto a água irá remover acidez do café.
Se o KH estiver abaixo de GH, então o teste KH fornece o valor tanto para a dureza temporária quanto para o alcalinidade, porque KH determina quanto de GH pode formar calcário. Se o KH estiver acima do GH, então o KH apenas mede o alcalinidade, e a dureza temporária é igual à dureza total, porque o KH 'extra' não pode se formar calcário por si próprio.





Com base na explicação, estou perplexo por que existe esta isenção de responsabilidade sobre o uso de receitas de água - “NB: Se você estiver fazendo sua própria água com sais de magnésio (como sais de Epsom), então o cálculo LSI não se aplica como não cálcio está presente. Não recomendamos o uso deste tipo de água em máquinas de café expresso.” –
Esta página menciona que o magnésio se liga aos carbonatos presentes, o que resulta em KH (dureza temporária). Isto formará levemente incrustações e isso é bom, de acordo com uma das respostas acima, isso cria um bom ciclo onde uma fina camada de calcário protetor é formada na caldeira que troca continuamente com a nova água remineralizada sendo adicionada como o a água ferve e esfria.
Meu objetivo é criar água com um ótimo sabor, mas que também seja segura para uso em uma máquina de café expresso. Posso usar as receitas deste URL com segurança? https://www.baristahustle.com/app-archive-main/the-water-calculator/
Olá Samizzle. O problema é que, se você criar uma água de café usando água destilada que não contenha nenhum cálcio, mesmo depois de adicionar seus sais de Epsom e seu bicarbonato por meio dos concentrados que recomendamos aqui https://www.baristahustle.com/blog/diy-water-recipes-redux/, é possível que esta água ainda não esteja formando incrustações e também possa ter o potencial de enferrujar partes da sua caldeira ou outros componentes. É por isso que criamos a calculadora de garrafas, para permitir a remineralização de uma água que contém uma quantidade conhecida de cálcio. Do course, você precisa ter cuidado para não acabar com uma água formando incrustações excessivas, então mesmo se você encontrar uma boa água base que possa conter, digamos, 30 miligramas / L de cálcio, de acordo com o rótulo da garrafa, certifique-se para testar seu GH também.
Interessante, estou descobrindo que quando pensei que entendi isso, não entendi absolutamente nada: S. Ainda estou tentando entender a diferença entre magnésio e cálcio em relação à produção de calcário, dada esta afirmação: “Como o cálcio e o magnésio têm duas cargas positivas, eles se comportam de maneira muito semelhante, portanto podem ser considerados intercambiáveis quando falamos sobre dureza.”
Você está dizendo que o carbonato de cálcio deposita calcário mais facilmente do que o carbonato de magnésio? Em caso afirmativo, é possível sugerir que quantidade de cálcio eu poderia adicionar ao meu 1L de concentrado de dureza (além dos 2,45g de sais de Epsom que já adicionei) para equilibrar isso adequadamente e evitar corrosão?
Está correto. O magnésio pode formar uma espécie de incrustação, mas não tende a aderir às superfícies da mesma forma que o calcário (o calcário é cálcio por definição).
O potencial de formação de incrustações da sua água (conforme medido pelo LSI) depende de mais do que apenas a quantidade de Ca – também depende do que mais está presente, do pH da água e até mesmo da temperatura. Portanto, não posso lhe dar uma recomendação específica, mas encorajo você a verificar o LSI da sua água com nosso Calculadora de Água.
Dito tudo isso, se a corrosão é um risco sério para a sua máquina ou não, depende do que ela é feita e de como é construída. Muitas máquinas funcionam com água destilada sem problemas durante muitos anos, outras podem apresentar corrosão mesmo com água natural. Para um pouco mais de informações sobre isso, confira o AMA que fizemos sobre água.
Excelente informação, obrigado. Eu tenho outra pergunta para você. Nossa água é relativamente dura, com 350-400 ppm. Estamos no processo de selecionar um amaciante de água para retirar os íons minerais ou um condicionador de água TAC para forçar a cristalização dos íons, mas não os remove. Como a presença desses cristais inertes afetaria a bebida?
Olá Dan, obrigado por comentar. Não temos experiência direta com TAC ou opções de tratamento de água relacionadas (como condicionadores de água magnéticos ou elétricos), mas estamos céticos.
Diz-se que a forma como este tipo de condicionador de água funciona é forçando a formação de microcristais de carbonato de cálcio - em outras palavras, minúsculos cristais de calcário. A teoria é que, ao formar cristais na água, você evita que eles se formem na superfície metálica do aquecedor de água.
É possível que o TAC possa ajudar a reduzir a formação de calcário como este em determinadas situações, mas o quão bem isto funciona na maioria dos ambientes do mundo real está longe de ser comprovado. Esta página tem uma boa visão geral do pouco que se sabe sobre eles e aponta para uma grande falha: os cristais só se formarão se a água estiver supersaturada – portanto, embora possa funcionar até certo ponto, pode não ser tão eficaz quanto um amaciante para obter aos níveis de dureza que gostamos para o café.
Como eles citam: “Não pode fazer nada para evitar a deposição de incrustações em superfícies de alta temperatura, onde os carbonatos serão menos solúveis, nem pode remover os íons de dureza até um nível em que não formarão espuma com sabão”. Suspeito que se a água ainda for dura o suficiente para formar uma espuma de sabão, será dura o suficiente para ter um efeito negativo no café. Também vale a pena ter em mente que esses cristais não são “inertes” – são simplesmente pequenos cristais de calcário e não há nada que impeça que sejam redissolvidos na água.
Se você – ou algum de nossos leitores – experimentar um condicionador TAC para o café, adoraríamos ouvir sobre sua experiência. Mas, por enquanto, recomendamos usar amaciantes ou unidades RO para ter certeza de bons resultados.
Sempre considero a água a parte mais intrigante e complexa do café. Pergunta: se a maior parte da água da torneira tem um nível mais baixo de HCO- do que Mg+ e Ca+, e quando a água é fervida todo o HCO- 'se emparelha' com Mg+ e Ca+ (formando calcário), como pode sobrar algum HCO- na água? água para reduzir sua acidez?
eu tenho a mesma pergunta que você. aguardo resposta de BH
Olá, Will – há duas coisas em jogo aqui.
A primeira é que leva tempo para a formação de calcário. Se você estiver fervendo uma chaleira para fazer café, apenas uma pequena quantidade de calcário se formará no momento em que você preparar o café, portanto ainda haverá bastante bicarbonato na água após a fervura. Você terá que ferver a chaleira por muito tempo para retirar todo o calcário.
Agora, numa máquina de café expresso, a chaleira ferve durante muito tempo – para sempre, se não a desligar. Mas neste caso, o segundo factor entra em jogo – o calcário existente na caldeira começa a dissolver-se também na água. Existe um ponto de equilíbrio onde a quantidade de calcário dissolvido é igual à quantidade formada – esta é a ideia por trás do Índice de Saturação Langelier, sobre o qual você pode ler mais em O Curso de Água.
Ah, obrigado, isso faz muito sentido. Então, ao manter a água em alta temperatura em um recipiente “limpo” por um longo tempo, você poderá eliminar mais bicarbonato, mas a filtração obviamente se torna uma opção mais sensata.
Ei! Há muito tempo que fico intrigado com uma pergunta simples: se as formas de Mg escalam tão bem quanto o Ca, por que Hendon e M CD defendem a substituição de Mg por Ca? Ou o Mg é de alguma forma “mais seguro” em termos de escala (dado que 95% de fontes alertam apenas sobre Ca, certamente parece que sim…)?
Olá, obrigado por postar isso – é uma boa pergunta.
A resposta curta é que eles acham que melhora o sabor. Eles propõem que o Mg extrai proporcionalmente mais dos compostos de sabor desejáveis. Isso se baseia em seus próprios testes de sabor e eles sugerem um mecanismo para isso por meio da química computacional (https://pubs.acs.org/doi/pdf/10.1021/jf501687c), mas até onde eu sei, isso não foi confirmado de forma independente.
A principal razão pela qual a maioria das fontes alerta sobre a incrustação de cálcio é que o cálcio é geralmente o principal componente da dureza da água potável, portanto a incrustação de magnésio não é um grande problema. No entanto, trocar o cálcio por magnésio também pode reduzir ligeiramente o impacto da incrustação. O magnésio interfere na estrutura cristalina da incrustação de carbonato de cálcio, tornando mais provável a formação de cristais de aragonita, que são ligeiramente mais solúveis que os cristais de calcita formados por carbonato de cálcio puro. O próprio Mg forma escamas de carbonato de magnésio e hidróxido de magnésio, mas ambos são um pouco mais solúveis que o hidróxido de cálcio a 100°C. Portanto, parece possível que ter uma proporção maior de magnésio também seja “mais seguro”.
Sim, obrigado pela resposta, é realmente útil! Isso é algo que ainda não encontrei.
“…mas ambos são um pouco mais solúveis que o hidróxido de cálcio a 100C” – você quer dizer CaCO3 aqui, certo?
Eu moro nos EUA e pelo que pude entender no relatório de qualidade da água do meu distrito hídrico local, parece que temos água muito dura. Então eu uso água engarrafada para fazer café. Me deparei com o jarro de água do pico. Eu queria saber se todos vocês já tiveram a chance de conferir.
Olá Timóteo. O filtro Peak Water analisa muito bem. Scott Rao o recomendou fortemente em seu boletim informativo recente de dezembro. Um comentário que ouvimos algumas vezes é que é menos consistente ao longo do tempo, mas isso é esperado com todos os sistemas de troca iônica.
Comparei o Peak com o jarro de filtro Brita Marella (usando cartuchos Maxtra). Ambos são quase igualmente eficientes em termos de troca iônica (o cartucho Brita foi um pouco usado, então fiz um desconto por isso), mas o TBH Brita parece muito mais sólido em termos de materiais e design. Peak tem essa sensação de plástico fabricado na China de baixa qualidade, infelizmente, e temo que não dure muito.