L'indice de saturation de Langelier
En 1936, le professeur WF Langelier de l'Université de Californie à Berkeley a rédigé un document de recherche . Il décrivait sa nouvelle méthode de calcul du pH auquel l'eau devient saturée de carbonate de calcium . Ce point de saturation est appelé pH. L'indice de saturation de Langelier (LSI), comme on l'a appelé, exprime la différence entre le pH réel d'un échantillon d'eau et le pH qu'il aurait s'il était saturé de carbonate de calcium .
Une lecture de zéro suggère qu'une eau est de l'eau qui a une lecture LSI de zéro. Cela signifie qu’il ne sera ni calcaire ni corrosif. " class="glossaryLink" target="_self">équilibré et ne se dissoudra pas ou ne risquera pas de se dissoudre . Le résultat d'une réaction qui rassemble deux substances dissoutes dans une solution pour former un solide insoluble. En devenant un solide, le nouveau la substance formée "précipite", c'est-à-dire qu'elle tombe au fond du récipient. " class="glossaryLink" target="_self">précipite le calcaire . Une lecture négative indique que l’eau est de l’eau ayant la capacité de dissoudre le carbonate de calcium. L’eau sous-saturée a un LSI inférieur à zéro et est susceptible d’être corrosive. " class="glossaryLink" target="_self">sous-saturé et a la capacité de dissoudre le carbonate de calcium . Une lecture très faible telle que -2 indique que l'eau est très susceptible de dissoudre le carbonate de calcium , et nous en déduisons que l'eau provoquera probablement la corrosion des chaudières et des tuyaux. Une lecture positive indique que l'eau est (de l'eau) de l'eau qui a un excès de dureté et d'alcalinité et donnera une lecture LSI supérieure à zéro. Cette eau est très susceptible de former du calcaire. " class="glossaryLink " target="_self">sursaturé en carbonate de calcium et sera Le résultat d'une réaction qui rassemble deux substances dissoutes dans une solution pour former un solide insoluble. En devenant solide, la substance nouvellement formée « précipite », c'est-à-dire qu'elle tombe au fond du récipient. " class="glossaryLink" target="_self"> calcaire précipité . Une lecture de 2, par exemple, indique une eau qui a tendance à laisser des dépôts importants de calcaire .
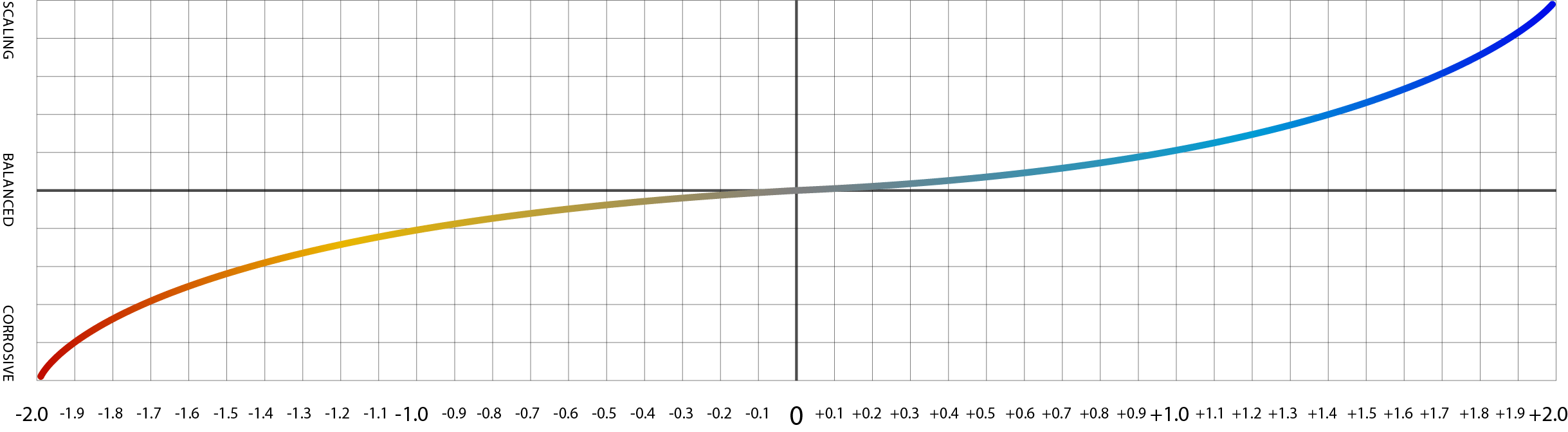
Une image de l'échelle de Langelier où les nombres négatifs indiquent la corrosivité et les nombres positifs indiquent le potentiel de formation de tartre.
Langelier a vu les avantages d'utiliser stratégiquement le potentiel de formation de tartre d'une eau saturée : son idée était d'utiliser le calcaire comme une sorte de revêtement en téflon. Dans son article de 1936, il déclare : « Le carbonate de calcium est le sel le plus utile pour la formation, ou avec la rouille, pour aider à la formation d'un revêtement auto-cicatrisant ou protecteur naturel. »
Si l’on s’inspire des recommandations de Scott Guglielmino (du précédent lesson), les valeurs LSI allant de 0,2 à 0,7 représentent un niveau sûr de saturation de l’eau qui favorisera une certaine formation de calcaire , mais pas excessive.
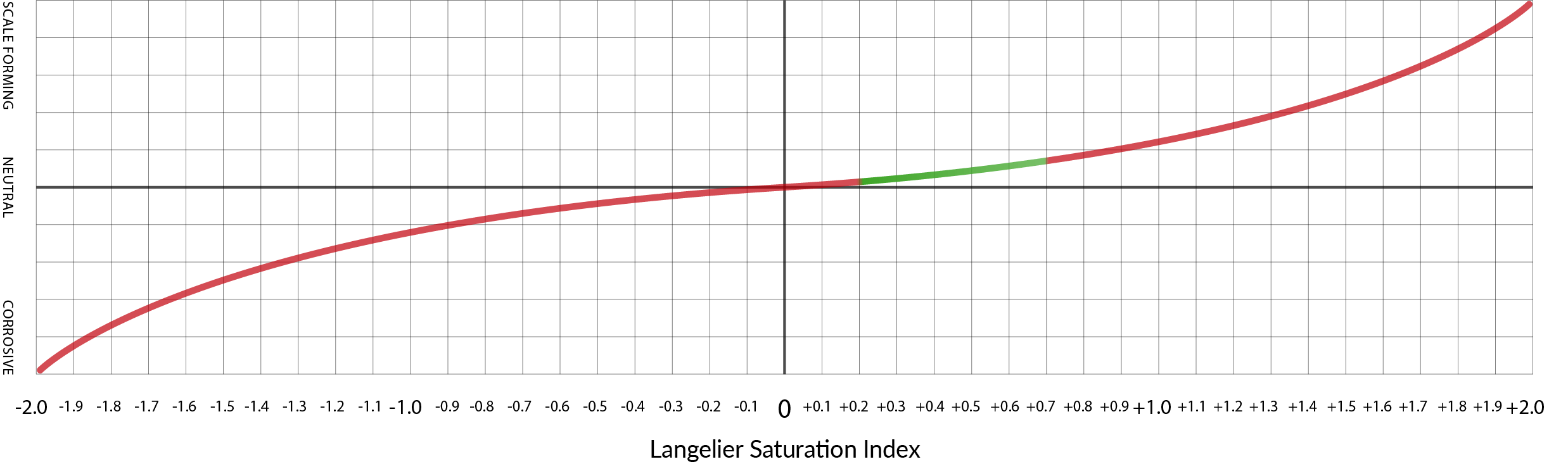
La section verte de cette illustration représente la plage d'eau potable de La Marzocco avec des valeurs LSI allant de 0,2 à 0,7.